La depresión se ha explicado durante décadas principalmente como un problema de neurotransmisores: desequilibrios en serotonina, dopamina o noradrenalina en el cerebro. Esa explicación funcionó suficientemente bien como para sostener décadas de farmacología, aunque los antidepresivos fallan en una porción significativa de los pacientes y nadie entiende del todo por qué.
Una hipótesis alternativa viene ganando terreno en la investigación reciente: la inflamación crónica, no los desequilibrios de neurotransmisores, podría ser la causa subyacente de muchos casos de depresión. Y si la inflamación es el mecanismo, entonces la pregunta siguiente es qué la desencadena.
Un estudio publicado por investigadores de Harvard Medical School en el Journal of the American Chemical Society propone una respuesta específica y sorprendente: una bacteria intestinal común, un contaminante industrial omnipresente, y una molécula que nadie había visto antes.
La cadena de tres pasos
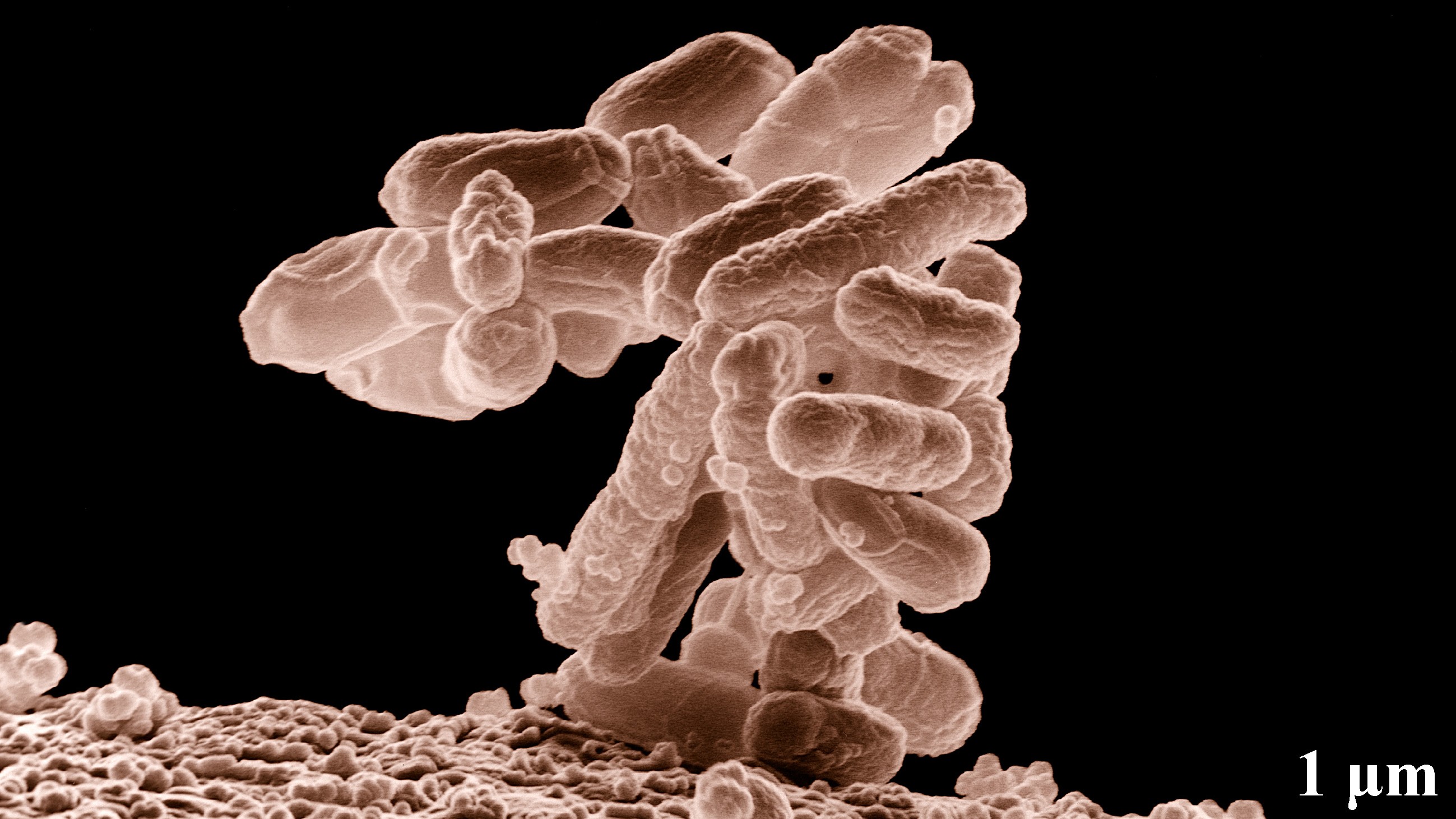
La bacteria se llama Morganella morganii. Es un residente habitual del intestino humano y había sido asociada previamente con enfermedades inflamatorias como la diabetes tipo 2 y la enfermedad inflamatoria intestinal. Estudios anteriores también la habían vinculado estadísticamente con el trastorno depresivo mayor, sin que nadie supiera exactamente por qué.
El contaminante se llama dietanolamina, o DEA. Es un compuesto industrial usado en cosméticos, detergentes, herbicidas y procesos industriales. Está presente en aguas residuales y en suelos agrícolas de todo el mundo.
El mecanismo que el equipo de Jon Clardy —Christopher T. Walsh Professor of Biological Chemistry en Harvard— descubrió es el siguiente: cuando la DEA entra en contacto con la Morganella morganii en el intestino, la bacteria la incorpora en una molécula que normalmente produciría con un ingrediente diferente, un alcohol de azúcar. La DEA reemplaza ese alcohol, creando una molécula alterada que el sistema inmune nunca había visto.
Esa molécula alterada —denominada MmDEACL— se une a dos receptores del sistema inmune, TLR1 y TLR2, y activa una respuesta inflamatoria. La respuesta incluye la liberación de citocinas, especialmente interleuquina-6 (IL-6), una proteína inflamatoria que múltiples estudios previos han asociado con el trastorno depresivo mayor.
Clardy describió el hallazgo con una sola frase: "El metabolismo de la DEA como señal inmune fue completamente inesperado."
Por qué esto cambia la imagen de la depresión
La depresión afecta a unos 280 millones de personas en el mundo, según la Organización Mundial de la Salud. Los antidepresivos actuales —inhibidores selectivos de la recaptación de serotonina, inhibidores de la recaptación de serotonina y noradrenalina— funcionan en una proporción significativa de los pacientes, pero hasta el 30 por ciento no responde adecuadamente a ningún tratamiento disponible.
La hipótesis inflamatoria de la depresión sugiere que al menos una parte de esos casos rebeldes al tratamiento podrían tener una causa distinta: no una disfunción en los circuitos de neurotransmisores sino una inflamación crónica de bajo grado que afecta la función cerebral a través de mecanismos que los antidepresivos convencionales no atacan.
El hallazgo de Harvard construye una cadena mecánica completa: DEA en el ambiente → M. morganii en el intestino → MmDEACL → activación inmune → IL-6 → inflamación → depresión. Cada eslabón de esa cadena es verificable experimentalmente. Es la diferencia entre una correlación estadística y una hipótesis mecanística.
El eje intestino-cerebro y sus implicaciones
La conexión entre el microbioma intestinal y la salud mental no es nueva como concepto. El llamado "eje intestino-cerebro" —la comunicación bidireccional entre el sistema nervioso central y los microbios que habitan el tracto digestivo— es objeto de investigación activa desde hace más de una década. Pero la mayor parte de esa investigación opera en el nivel de las correlaciones: ciertos patrones del microbioma se asocian con ciertos estados mentales, sin que se comprenda el mecanismo exacto.
Lo que distingue el trabajo de Clardy es precisamente eso: el mecanismo. No se dice que M. morganii se correlaciona con la depresión. Se muestra exactamente qué molécula produce cuando se expone a DEA, qué receptores activa esa molécula, qué citocinas libera esa activación, y por qué esas citocinas son relevantes para la depresión.
Eso abre posibilidades terapéuticas concretas. Si la DEA es el detonador, reducir la exposición a DEA —o identificar pacientes con altos niveles de MmDEACL como biomarcador— podría ser una forma de diagnosticar o prevenir ciertos casos de depresión. Si la IL-6 es el efector, medicamentos inmunomoduladores que bloquean esa citocina podrían funcionar como antidepresivos en un subgrupo específico de pacientes.
El contaminante que todos llevamos
La DEA no es un compuesto oscuro de laboratorio. Es un ingrediente activo o subproducto de una cantidad enorme de productos cotidianos: champús, acondicionadores, cremas de afeitar, detergentes para lavar ropa, herbicidas agrícolas. También se usa en la manufactura de plásticos y en el tratamiento de gases en plantas industriales.
Los niveles de DEA en agua y suelo son medibles en regiones agrícolas e industriales del mundo. La exposición humana ocurre a través de productos de consumo, de agua contaminada y de la cadena alimentaria.
El estudio no cuantifica exactamente cuánta DEA llega al intestino en condiciones cotidianas, ni qué proporción de las personas con M. morganii en su microbioma tienen niveles detectables de MmDEACL. Esas preguntas son el siguiente paso de la investigación.
Lo que sí establece es el principio: un compuesto industrial omnipresente puede ser transformado por una bacteria intestinal en una señal inflamatoria que afecta la salud mental. La distancia entre el ambiente y el cerebro es más corta de lo que se pensaba.
Fuente original: JACS / ScienceDaily / Harvard Medical School