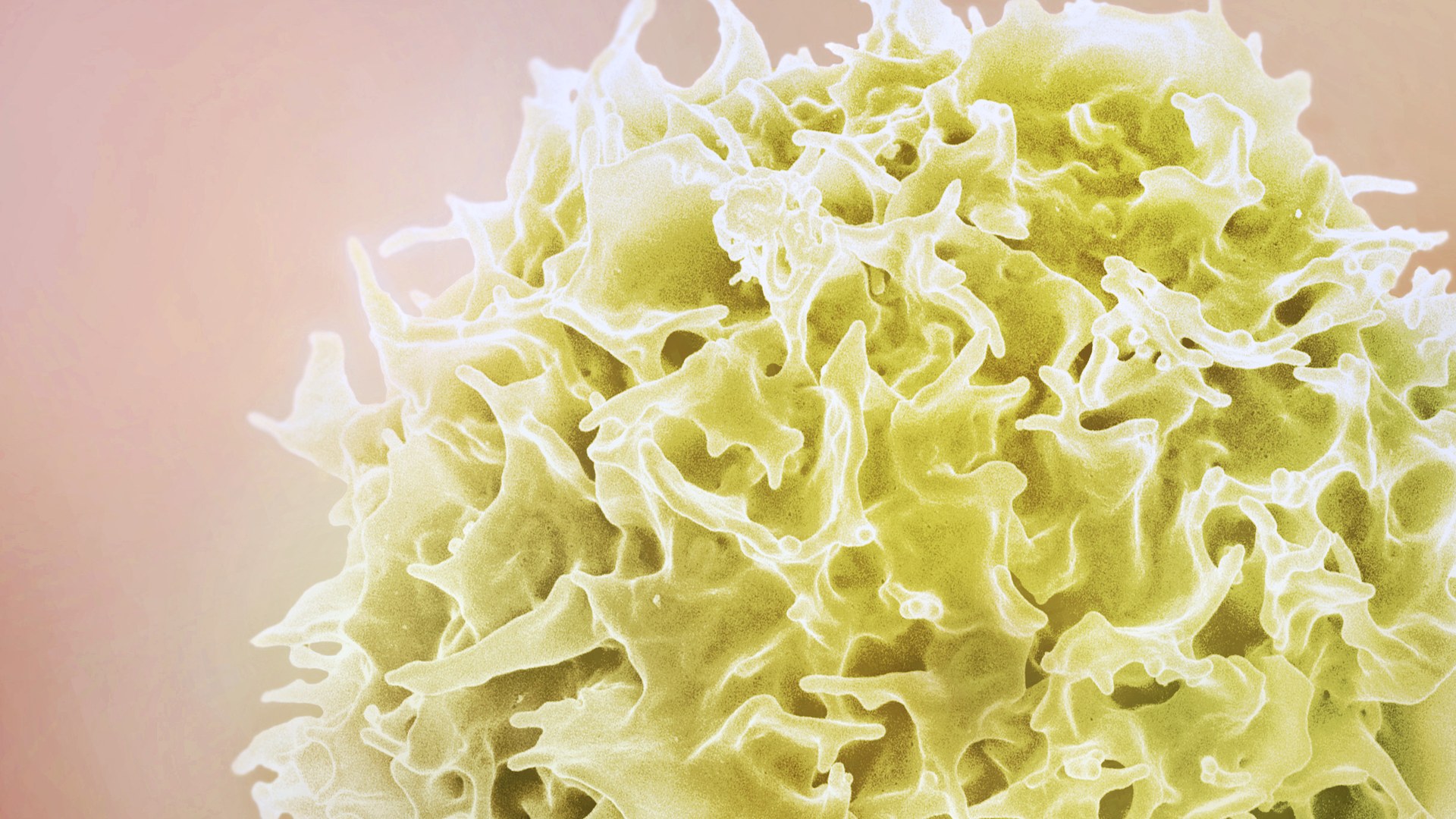
El sistema inmune tiene una división de élite. Se llama linfocitos T citotóxicos, también conocidos como células T asesinas, y su función es precisa: detectar células propias del organismo que se han vuelto peligrosas —infectadas por un virus, o cancerosas— y destruirlas sin dañar al tejido sano circundante. Son la unidad de combate más sofisticada que la evolución produjo para la defensa del cuerpo.
Desde hace décadas se sabe que estas células, para matar a su objetivo, establecen un contacto físico directo con la célula blanco y forman en ese punto de unión una estructura llamada sinapsis inmune. Por esa sinapsis liberan moléculas tóxicas que perforan y destruyen la célula amenazante. Lo que nadie había podido ver con detalle suficiente era exactamente cómo se organiza esa sinapsis en tres dimensiones, en condiciones próximas a las del tejido real.
Investigadores de la Université de Genève y del Hospital Universitario de Lausana publicaron el 30 de abril de 2026 en Cell Reports los resultados de un experimento que logró, por primera vez, imágenes tridimensionales de la sinapsis inmune a escala nanométrica. Y lo que vieron tiene consecuencias directas para entender por qué la inmunoterapia contra el cáncer funciona bien en algunos pacientes y falla en otros.
El problema técnico que bloqueaba la visión
Observar la sinapsis inmune en detalle tiene un obstáculo fundamental: la escala. Los procesos relevantes ocurren en rangos de decenas a cientos de nanómetros — un nanómetro es un millonésimo de milímetro. La microscopía óptica convencional no tiene resolución suficiente. La microscopía electrónica tiene la resolución necesaria pero requiere condiciones de preparación de muestras que alteran profundamente la arquitectura de las células vivas.
El equipo liderado por Virginie Hamel, del Departamento de Biología Celular de la Universidad de Ginebra, resolvió el problema combinando dos técnicas de maneras que no se habían hecho antes. La primera es la criomicroscopía: las células se congelan instantáneamente a velocidades extremas, llevando el agua intracelular a un estado vítreo donde solidifica sin formar cristales de hielo. Eso preserva la arquitectura biológica en una condición muy próxima a la natural. La segunda es la microscopía de expansión: las muestras se embeben en un hidrogel absorbente que, al hincharse, expande físicamente la estructura celular preservada, separando las estructuras nanométricas lo suficiente como para resolverlas con un microscopio óptico de alta resolución.
La técnica combinada —llamada cryo-expansion microscopy, o Cryo-ExM— permite ver estructuras que antes eran invisibles en condiciones próximas al estado nativo de las células. Florent Lemaître, investigador postdoctoral y primer autor del trabajo, describió el resultado: "Esta técnica permite congelar instantáneamente las células a muy alta velocidad, colocándolas en un estado vítreo donde el agua solidifica sin formar cristales y preserva fielmente las estructuras biológicas."
La cúpula que nadie había visto
El hallazgo más llamativo es la geometría de la sinapsis. En el punto de contacto entre la célula T y su objetivo, la membrana de la célula asesina no forma una interfaz plana, como se representaba en los esquemas habituales. Forma una cúpula. Una estructura tridimensional que envuelve parcialmente a la célula blanco, cuya forma parece estar determinada tanto por las interacciones de adhesión entre ambas células como por la organización interna del citoesqueleto de la célula T.
Esa cúpula tiene implicaciones funcionales. La geometría del contacto determina cómo se concentran y dirigen las moléculas tóxicas que la célula T libera para matar a su objetivo. Un contacto más o menos envolvente, más o menos simétrico, puede afectar la eficiencia con que esas moléculas alcanzan la membrana de la célula blanco.
Los gránulos que llevan los venenos
La célula T destruye su objetivo mediante moléculas especializadas que almacena en estructuras intracelulares llamadas gránulos citotóxicos. Los principales efectores son la perforina —que literalmente perfora la membrana de la célula blanco creando poros— y el granzyme B, una enzima que entra por esos poros y activa las vías de autodestrucción de la célula infectada o cancerosa.
Las imágenes de Cryo-ExM revelaron que estos gránulos no son uniformes. Tienen una organización interna con uno o múltiples núcleos donde se concentran las moléculas activas. Esa variedad estructural no era visible con las técnicas anteriores y sugiere que distintos gránulos pueden tener distintas capacidades o tiempos de liberación. La heterogeneidad de los gránulos dentro de una misma célula T podría ser parte de la manera en que el sistema inmune gradúa su respuesta.
Del laboratorio al tumor humano real
Lo que distingue a este trabajo de estudios similares es que el equipo no se limitó a células cultivadas en condiciones artificiales. Benita Wolf, médica residente en el Hospital Universitario de Lausana y co-autora del estudio, extendió la técnica a muestras de tumores humanos reales. Las imágenes resultantes muestran linfocitos T infiltrando tejido tumoral real, con su maquinaria citotóxica visible a escala nanométrica, en el entorno biológico complejo de un tumor.
Esa extensión transforma el alcance del método. La técnica trasciende el laboratorio básico: es una forma de examinar directamente cómo funciona —o falla— la respuesta inmune dentro de los tumores de pacientes concretos.
La brecha entre inmunoterapia eficaz e ineficaz
La inmunoterapia contra el cáncer es uno de los avances terapéuticos más importantes de las últimas décadas. Los llamados inhibidores de puntos de control inmune —medicamentos que liberan al sistema inmune de los frenos que los tumores le imponen— transformaron el pronóstico de varios tipos de cáncer que antes tenían tratamientos muy limitados. Las terapias CAR-T, que toman células T del paciente, las modifican genéticamente para reconocer células tumorales específicas y las reinfunden, extendieron ese alcance.
El problema es que la inmunoterapia funciona bien en una minoría de pacientes y no funciona en la mayoría. Las razones de esa variabilidad son parcialmente conocidas —el microambiente tumoral supresor, la heterogeneidad del tumor, el agotamiento de las células T— pero los mecanismos celulares precisos siguen siendo materia de investigación activa.
Ver la sinapsis inmune en 3D dentro de tejido tumoral real abre una manera nueva de estudiar esa pregunta. Si una célula T bien formada con una sinapsis completa y gránulos bien organizados mata eficazmente a las células tumorales que la rodean pero otra no, esa diferencia se puede ahora observar directamente y relacionar con las condiciones del microambiente tumoral. Es la diferencia entre inferir lo que ocurre y verlo.
Fuente original: Cell Reports / ScienceDaily / Université de Genève