El sentido del olfato es, entre los sentidos humanos, el que mejor resistió durante décadas la comprensión científica. Sabemos con bastante precisión cómo funciona la visión: hay células fotorreceptoras en la retina, sensibles a longitudes de onda específicas de luz, conectadas a una arquitectura neuronal bien mapeada. El oído también tiene su mapa: el órgano de Corti en la cóclea es una estructura topográfica donde las células ciliadas responden a frecuencias distintas según su posición. Pero el olfato era diferente. La pregunta básica —cómo están organizados los receptores olfativos en la nariz— no tenía respuesta.
Hasta ahora.
Un estudio publicado el 28 de abril de 2026 en la revista Cell, producto de dos equipos independientes de Harvard que trabajaron en paralelo y encontraron resultados consistentes, reveló por primera vez que los receptores del olfato no están distribuidos de manera aleatoria en el epitelio nasal. Están organizados en un mapa preciso. Y ese mapa se corresponde, con notable exactitud, con el mapa que existe en el bulbo olfativo del cerebro.
El problema que nadie había resuelto
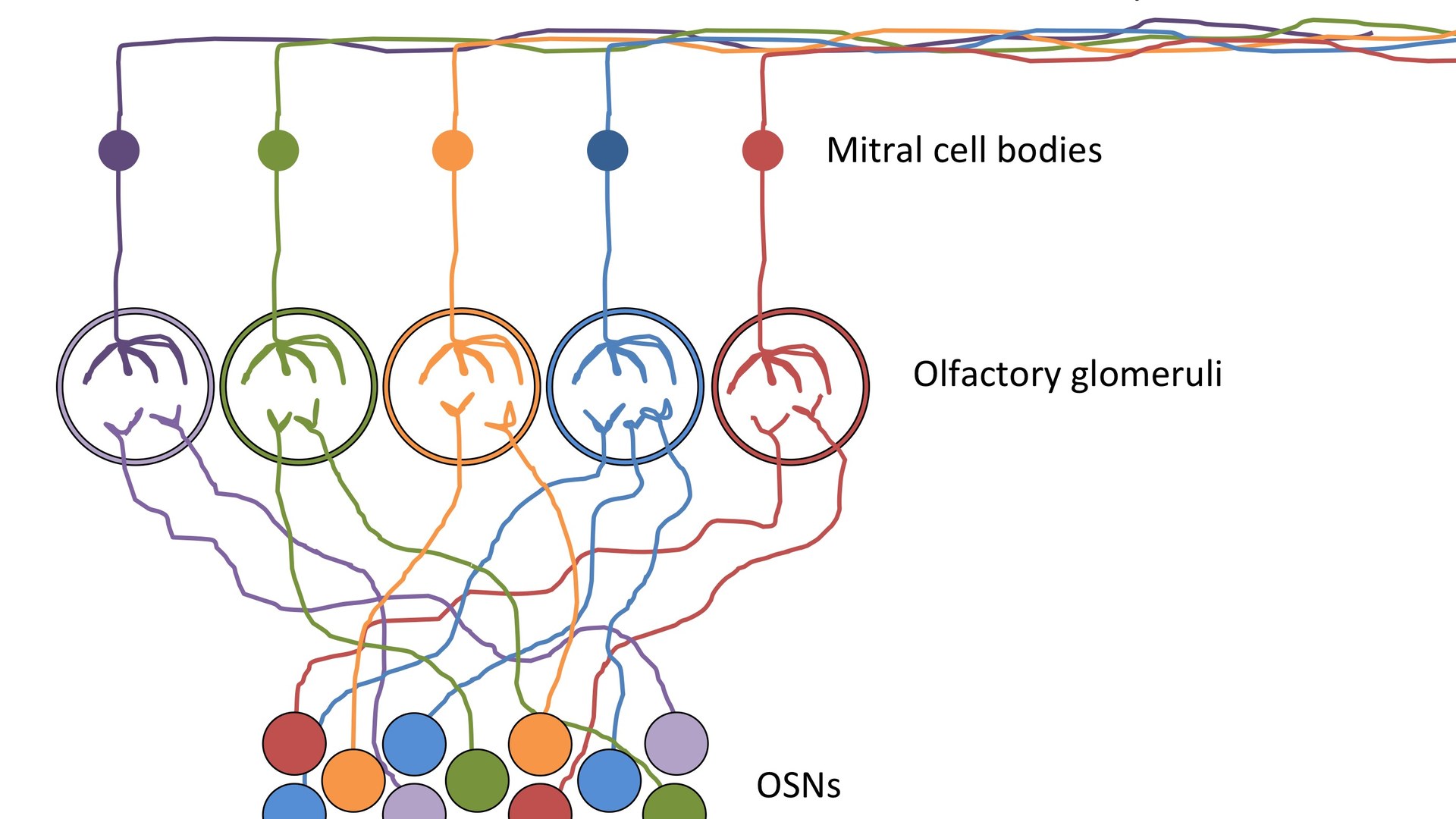
La nariz de los ratones —el modelo animal usado en este estudio— contiene alrededor de 1.100 tipos distintos de receptores olfativos. Cada neurona olfativa expresa solo uno de esos receptores. Durante mucho tiempo, se asumió que esa distribución era esencialmente aleatoria: distintas neuronas con distintos receptores mezcladas sin patrón reconocible a lo largo del epitelio nasal.
Ese supuesto tenía lógica. La retina tiene estructura porque la luz viaja en línea recta y el sistema visual necesita preservar la geometría espacial de lo que se ve. El oído tiene estructura porque las frecuencias sonoras son continuas y ordenables. Pero ¿el olfato? Las moléculas odorantes no tienen una dimensión espacial obvia que justifique un mapa. ¿Por qué el cerebro necesitaría que el receptor del olor a rosa esté en una posición específica de la nariz y el del café en otra?
La respuesta que emergió del estudio no es sobre lógica funcional: es sobre biología del desarrollo.
Cinco millones y medio de neuronas, trescientos ratones
El equipo liderado por Sandeep Datta en Harvard Medical School empleó dos técnicas complementarias de manera conjunta: secuenciación de células individuales y transcriptómica espacial. La primera permite identificar qué receptor expresa cada neurona. La segunda permite determinar en qué posición exacta de la nariz está ubicada esa neurona.
El equipo de Catherine Dulac y Xiawei Zhuang, en el Departamento de Biología Molecular y Celular de Harvard, usó una técnica aún más precisa: MERFISH (Multiplexed Error-Robust Fluorescent In Situ Hybridization), un método de transcriptómica espacial desarrollado en el propio laboratorio de Zhuang que permite visualizar la expresión génica directamente en tejido intacto con resolución submicrónica.
Juntos, los dos grupos analizaron aproximadamente 5,5 millones de neuronas distribuidas en más de 300 ratones individuales. El resultado fue el primer atlas completo del epitelio nasal a nivel molecular.
Lo que encontraron contradijo décadas de suposición: las neuronas que expresan cada tipo de receptor forman bandas horizontales ordenadas. Hay una organización topográfica clara, tanto a lo largo del eje dorso-ventral de la nariz como en el eje basal-apical. Y esa organización es, además, notablemente consistente entre distintos animales. El mapa no es caótico ni individual: es una característica de la especie.
El ácido retinoico como guía del desarrollo
¿Qué establece ese orden durante el desarrollo embrionario? El equipo de Datta identificó al ácido retinoico como el factor clave. Este compuesto —derivado de la vitamina A— forma un gradiente de concentración en el epitelio nasal durante el desarrollo: más concentrado en algunas zonas, menos en otras. Ese gradiente actúa como un sistema de coordenadas: le dice a cada neurona, según su posición, qué tipo de receptor debe activar.
Cuando los investigadores manipularon ese gradiente —añadiendo o eliminando ácido retinoico en el desarrollo— el mapa de receptores se desplazó correspondientemente arriba o abajo. La geometría del mapa es controlable porque responde a señales moleculares precisas.
El hallazgo del bulbo olfativo complementa esto de manera elegante. Bogdan Bintu, investigador principal del estudio y hoy profesor asistente en UC San Diego, describió la conectividad: "Estas neuronas son notables porque hay alrededor de mil tipos distintos en el ratón, y cada tipo expresa un solo receptor olfativo y envía su axón a una ubicación muy específica en el cerebro." Lo que el estudio establece ahora es que esa ubicación específica en el cerebro se corresponde con la posición geográfica de la neurona en la nariz: la organización espacial se preserva y transforma con precisión a lo largo de la vía olfativa.
Por qué hay un mapa y para qué sirve
La pregunta conceptual que sigue abierta es por qué el olfato necesita esta organización topográfica. El equipo de Dulac y Zhuang encontró una pista funcional: cuando midieron la actividad de distintas zonas del epitelio en respuesta a olores biológicamente relevantes —señales sociales, olores de depredadores, señales de crías— distintas categorías de olores activaron dominios espaciales distintos en la nariz.
Eso sugiere que el mapa no es ornamental: podría ser la forma en que el sistema olfativo separa tipos de información desde el primer nivel de procesamiento, antes incluso de llegar al cerebro. El sistema parece optimizado para enrutar distintas categorías de información hacia circuitos específicos que generan comportamientos muy diferentes.
Las implicancias para tratar la pérdida del olfato
La pérdida del olfato —anosmia— afecta a millones de personas en el mundo. Puede ser consecuencia de infecciones virales (como ocurrió masivamente con COVID-19), de lesiones en la cabeza, de enfermedades neurodegenerativas o simplemente del envejecimiento. Tiene consecuencias que van más allá de lo que suele reconocerse: afecta la seguridad (las personas no perciben gas o humo), la nutrición (el placer de comer depende en gran medida del olfato), y la salud mental (la pérdida del olfato se asocia consistentemente con mayor riesgo de depresión).
Hasta ahora, el problema de tratar la pérdida del olfato era en parte conceptual: sin saber cómo están organizados los receptores, era difícil diseñar estrategias para repoblarlos o repararlos. Datta fue directo sobre ese punto: "No podemos arreglar el olfato sin entender primero cómo funciona en un nivel básico."
El nuevo atlas abre vías concretas. Si los receptores están organizados de manera específica y ese orden es controlado por señales moleculares como el ácido retinoico, entonces las terapias de células madre para regenerar el epitelio olfativo podrían diseñarse para respetar esa arquitectura. Las interfaces cerebro-computadora para el olfato —todavía en etapa muy experimental— también necesitan entender el mapa para estimular las posiciones correctas.
Los dos atlas —el del equipo de Datta y el del equipo de Dulac y Zhuang— se publican como recursos abiertos para la comunidad científica. El siguiente paso es aplicar las mismas técnicas a tejido humano postmortem, para determinar en qué medida el mapa del ratón se corresponde con el mapa en la nariz de las personas. Si la organización es conservada evolutivamente, lo que se aprendió en ratones puede traducirse directamente en medicina.
Fuente original: Cell / ScienceDaily / Harvard / Harvard MCB