En 1961, Leonard Hayflick hizo una observación que cambió la biología del envejecimiento. Estaba cultivando células humanas en laboratorio y notó que dejaban de dividirse después de un número determinado de divisiones: alrededor de 50, con variaciones. Las células no morían de inmediato — se volvían inactivas, en un estado que hoy se llama senescencia. Y ese número máximo de divisiones, el límite de Hayflick, era constante e independiente del tiempo transcurrido.
Eso sugería que el envejecimiento no era solo desgaste acumulado. Había un límite biológico programado.
Décadas después, Elizabeth Blackburn, Carol Greider y Jack Szostak descubrieron el mecanismo detrás del límite de Hayflick: los telómeros. Su trabajo les valió el Nobel de Medicina en 2009.
Los telómeros: el reloj molecular
Los telómeros son secuencias repetitivas de ADN en los extremos de los cromosomas. Funcionan como las puntas plásticas de los cordones de las zapatillas: protegen los extremos del cromosoma para que no se deshilache y no se fusione con otros cromosomas.
Cada vez que una célula se divide, el ADN debe copiarse. Pero la maquinaria de copia del ADN — la ADN polimerasa — no puede replicar el extremo final del cromosoma. Esto se llama el "problema del extremo". El resultado es que con cada división celular, los telómeros se acortan un poco.
Cuando los telómeros llegan a una longitud crítica, la célula detecta la situación y activa señales que la llevan a la senescencia o la apoptosis (muerte celular programada). La célula deja de dividirse.
Hay un antídoto parcial: la enzima telomerasa, que puede reconstruir los telómeros. Las células madre y las células reproductivas tienen alta actividad de telomerasa. La mayoría de las células somáticas adultas tienen poca. Las células cancerosas, en cambio, reactivan la telomerasa — y por eso pueden dividirse sin límite.
No solo los telómeros
Los telómeros son uno de los mecanismos del envejecimiento, pero no el único. La biología del envejecimiento identifica hoy nueve "marcas del envejecimiento" (hallmarks of aging), descritas en un paper seminal de 2013 que fue actualizado en 2023 con doce marcas:
Inestabilidad genómica: La acumulación de daño en el ADN —por radiación, errores de copia, radicales libres— y la reducción de la eficiencia de los sistemas de reparación del ADN con la edad.
Epigenética alterada: Los patrones de metilación del ADN cambian con la edad de manera consistente. Steve Horvath desarrolló en 2013 el "reloj epigenético", que puede predecir la edad biológica con precisión a partir de estos patrones de metilación.
Disfunción proteostática: Las proteínas mal plegadas se acumulan con la edad. El sistema que las elimina —el ubiquitin-proteasoma y la autofagia— se vuelve menos eficiente. Las enfermedades neurodegenerativas como Alzheimer y Parkinson están fuertemente asociadas con acumulación de proteínas mal plegadas.
Senescencia celular: Las células senescentes no mueren, sino que permanecen activas y liberan sustancias inflamatorias — las llamadas SASP (secretome associated senescence phenotype). Esa inflamación crónica de bajo grado asociada al envejecimiento se llama "inflammaging".
Disfunción mitocondrial: Las mitocondrias, que generan la energía celular, se vuelven menos eficientes y producen más radicales libres con la edad. El ADN mitocondrial, que se replica de manera independiente del ADN nuclear, acumula mutaciones más rápidamente.
Agotamiento de células madre: Con la edad, los nichos de células madre se agotan y la capacidad regenerativa de los tejidos disminuye.
Por qué envejece el cerebro
El cerebro envejece de manera diferente a otros tejidos porque la mayoría de las neuronas no se reemplazan. Las neuronas que se tienen al nacer son en gran parte las mismas que se tienen a los 80 años — solo que con decenios de desgaste acumulado y, en el mejor de los casos, con nuevas conexiones formadas por la experiencia.
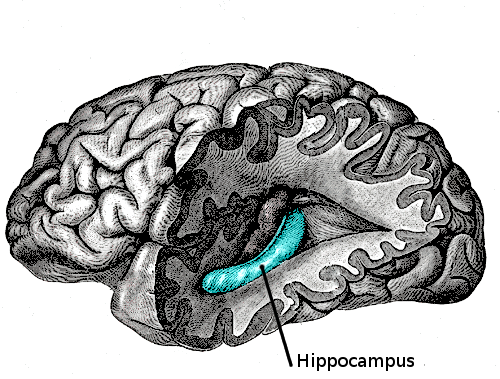
Los cambios principales en el cerebro envejecido incluyen reducción del volumen de la corteza prefrontal y el hipocampo, disminución de la densidad sináptica, acumulación de proteínas anormales como beta-amiloide (asociada al Alzheimer) y alfa-sinucleína (asociada al Parkinson), y reducción del flujo sanguíneo cerebral.
La velocidad del envejecimiento cerebral es altamente variable entre individuos. El concepto de "reserva cognitiva" — la resiliencia del cerebro ante el daño — está asociado con nivel educativo, complejidad de las actividades cognitivas a lo largo de la vida y redes sociales activas.
Qué puede retrasarlo (con evidencia)
La investigación sobre intervenciones que extienden la vida sana es extensa y a veces contradictoria, pero hay ciertos factores con evidencia repetida:
- Restricción calórica: Demostrada en animales —desde gusanos hasta primates— como la intervención más consistente para extender la vida. El mecanismo principal es la activación de vías como mTOR y AMPK que regulan el metabolismo celular. La evidencia en humanos es más limitada.
- Ejercicio físico: El que más impacto documentado tiene en múltiples marcas del envejecimiento. Activa la biogénesis mitocondrial, estimula BDNF, promueve la autofagia.
- Sueño: La privación crónica de sueño acelera múltiples marcas del envejecimiento. El sueño es cuando el sistema glinfático limpia proteínas de desecho del cerebro.
- No fumar: El tabaco acelera el acortamiento de telómeros a un ritmo medible.
Las drogas más prometedoras en investigación —rapamicina, metformina, senolytics— muestran efectos en animales pero no tienen evidencia suficiente en humanos todavía para recomendar su uso en personas sanas.
El límite de lo que se puede cambiar
La biología del envejecimiento progresó enormemente en los últimos 30 años. Pero hay una distinción importante entre entender el mecanismo y poder modificarlo de manera segura. Muchas de las vías del envejecimiento están conectadas con vías de protección contra el cáncer o con funciones esenciales del metabolismo.
La telomerasa, por ejemplo, reconstituye los telómeros, pero también facilita la inmortalidad celular del cáncer. Activarla en tejidos sanos es un arma de doble filo que todavía no se sabe manejar con seguridad.
Lo más honesto que puede decir la ciencia hoy es: hay mucho que retrasa el envejecimiento patológico. No hay todavía nada que lo revierta de manera segura y demostrada en humanos.
¿Por qué envejecemos? ¿Qué dice la ciencia hoy?
El envejecimiento no tiene una sola causa sino varios mecanismos que se acumulan. Los más documentados: el acortamiento de los telómeros (las "tapas" protectoras de los cromosomas que se acortan con cada división celular), la acumulación de células senescentes (células que dejaron de dividirse pero no mueren y liberan señales inflamatorias), el deterioro mitocondrial y el daño en el ADN que el sistema de reparación celular ya no puede corregir a la misma velocidad. La senescencia celular y la inflamación crónica de bajo grado son los mecanismos más activos en la investigación actual.
¿Se puede revertir o frenar el envejecimiento?
Frenarlo parcialmente sí, revertirlo de manera segura en humanos no todavía. Ejercicio aeróbico regular, sueño suficiente, dieta variada sin exceso calórico y no fumar son los factores con más evidencia para retrasar el envejecimiento patológico. Las drogas más investigadas —rapamicina, metformina, senolytics— muestran efectos claros en animales pero no tienen evidencia suficiente en humanos para recomendarlas en personas sanas. La telomerasa es prometedora pero activa también vías del cáncer, lo que hace difícil usarla de manera segura.
¿Cuánto influye la genética en cuánto vivimos?
La genética explica aproximadamente el 25-30% de la variación en la longevidad, según estudios en gemelos. El resto es ambiental: hábitos, contexto socioeconómico, acceso a salud y factores aleatorios de exposición a enfermedades. Los genes asociados con longevidad extrema (centenarios) incluyen variantes del gen APOE y genes relacionados con el sistema cardiovascular e inflamatorio. Pero ningún gen garantiza larga vida, y los factores de estilo de vida tienen un efecto comparativamente mayor de lo que la mayoría asume.
Fuente original: Un Mundo Loco